Omvoh長期數據顯示四年63.5%維持疾病清除,安全性無新警訊,增強市場與臨床信心。
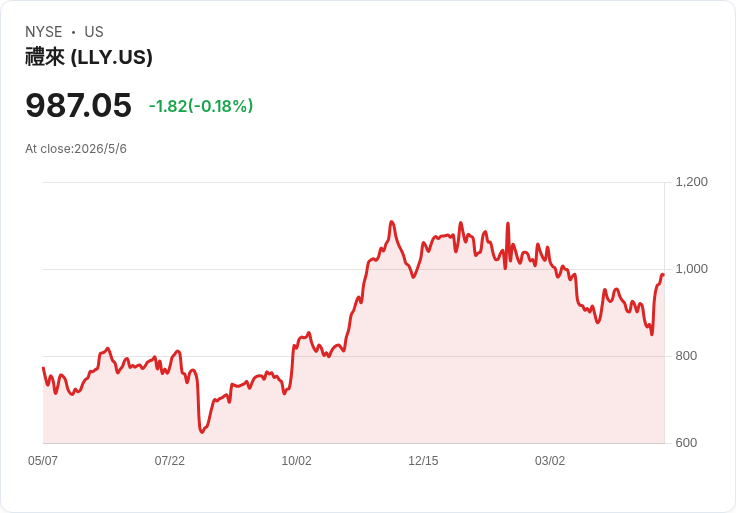
Eli Lilly(禮來)週二股價上揚,因公司公佈其治療潰瘍性結腸炎(UC)藥物Omvoh(mirikizumab‑mrkz)在長期追蹤中的正面資料,投資人與臨床界皆提高對藥物長效性的信心。
背景與核心資料: Omvoh在LUCENT‑2維持期達到臨床緩解的病人,續入開放標籤延伸研究LUCENT‑3接受長期追蹤。最新公佈結果指出,接受Omvoh治療並在一年時達到疾病清除的患者中,有63.5%在四年時仍維持疾病清除;以最嚴格的衡量標準(包含內視鏡正常、症狀與組織學緩解)計算,仍有61.3%維持至四年。安全性方面,在從LUCENT‑2轉至LUCENT‑3的病人中,有12%報告嚴重不良事件,7%因不良事件停藥;研究團隊表示未發現新的安全性警訊。
為何重要: 這組結果意義重大,因為Omvoh屬於第一類示範在UC中達到如此持久「疾病清除」的IL‑23p19抑制劑。長期維持疾病清除不僅提升病人生活品質,也可降低反覆用藥、住院與手術需求,對醫療成本與藥廠長期營收都有正面影響。先前Omvoh在2023年10月取得美國用於中度至重度潰瘍性結腸炎之核准,並在2025年1月獲批治療中度至重度克隆氏症,代表禮來已在兩大發炎性腸病領域取得重要法規里程碑。
補充臨床證據: 禮來此前也在克隆氏症的相關資料中報告長期效益:在另一項研究中超過90%的病人在三年內維持無類固醇緩解;Phase 3 VIVID‑2研究亦報告臨床緩解率92.4%、無類固醇臨床緩解91.2%,進一步支撐Omvoh在IBD族群的療效延續性。
對投資人與醫療界的分析: 短期來看,這類長期陽性資料有助鞏固禮來在IBD市場的領先地位,可能推動處方、市佔與營收成長;保險給付與藥價談判也會以長期有效減少醫療負擔為論點。從臨床角度,若真能在更大規模與真實世界資料中重現,Omvoh或成為改變治療路徑的選項。
可能的疑慮與反駁: 批評者會指出延伸研究屬開放標籤、選擇偏差(僅包含一年已達緩解的病人)可能高估長期效果;此外,樣本選擇、隨訪流失與實務中依從性都會影響結果外推性。對此,支持者強調資料仍以「要求內視鏡正常」等嚴格標準衡量,且安全性未見新警訊,顯示療效與風險的平衡具說服力。最終仍需更多頭對頭試驗與大型真實世界研究確認。
結論與展望: Omvoh四年資料為禮來在IBD市場加分,但未來觀察重點包括更廣泛族群的真實世界效益、長期安全監測、保險給付策略與與其他生物製劑之比較試驗。投資者與醫療決策者應追蹤後續發表、藥價談判與上市後監測結果,以評估其對公司財務與臨床照護路徑的持續影響。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37