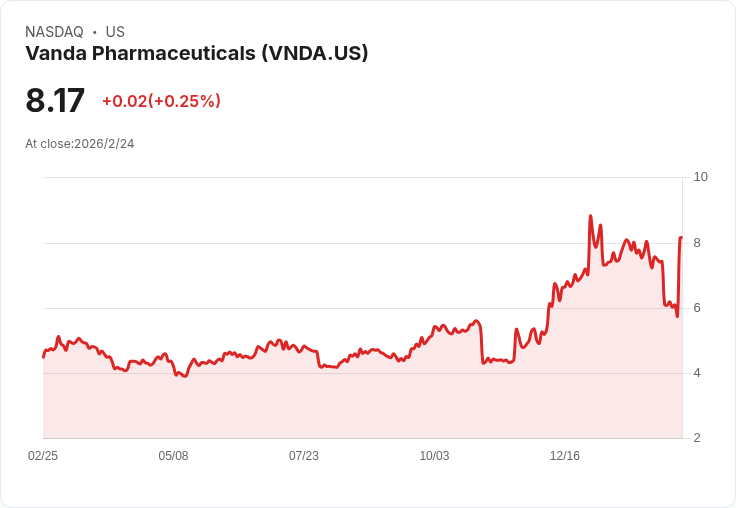
Vanda Pharmaceuticals的imsidolimab藥物已獲得美國FDA審查,針對罕見皮膚疾病「廣泛性膿皰型牛皮癬」,預計於2026年12月做出決定。
Vanda Pharmaceuticals(VNDA)週三在盤前交易中股價上漲約4%,因為公司宣佈其針對罕見皮膚病「廣泛性膿皰型牛皮癬」的治療藥物imsidolimab已獲得美國食品藥品監督管理局(FDA)的審查。此項生物製劑許可申請(BLA)目標行動日期定於2026年12月12日,並且有多項全球臨床試驗資料支援,包括GEMINI-1和GEMINI-2研究。
根據這兩項關鍵試驗的資料顯示,53%的使用imsidolimab的患者在四週內能夠耐受該藥物,並且皮膚狀況明顯改善至清晰或幾乎清晰,相較之下,僅有13%的安慰劑組達到相同效果。如果FDA作出正面決定,將是Vanda在過去一年中的第三次監管批准,此前該公司分別在去年12月和本月獲得了與Lilly合作的暈車藥Nereus及抗精神病藥片Bysanti的批准。
展望未來,若imsidolimab獲批,將為無法有效控制該皮膚病的患者帶來新的治療選擇,進一步鞏固Vanda在市場上的地位。同時,業界也在關注其他相關藥物的研發進度,以應對不斷增長的患者需求。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37