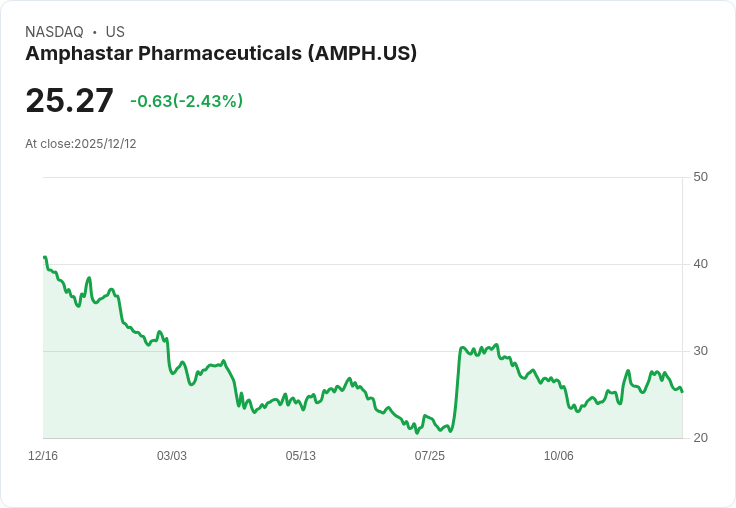
Amphastar獲得FDA批准其teriparatide注射劑,預計將於年底上市,市場銷售潛力高達5.85億美元。
Amphastar Pharmaceuticals(AMPH)今日宣佈,其針對治療骨質疏鬆症的teriparatide注射劑已獲得美國食品藥品監督管理局(FDA)的批准。該產品為單患者使用的預填充筆,劑量為560 mcg/2.24mL(250 mcg/mL)。FDA確認Amphastar的teriparatide在生物等效性和治療效果上均與Eli Lilly的FORTEO相當。
根據IQVIA的資料,2025年9月30日止的12個月內,美國市場上teriparatide注射劑的總銷售額約為5.85億美元。這顯示出該產品在市場中的巨大潛力,並可能成為Amphastar未來增長的重要推動力。
Amphastar計畫在今年底正式推出其teriparatide注射劑,該訊息也使得公司股價在盤前交易中上漲了4.8%。隨著市場需求不斷增加,Amphastar有望在競爭激烈的醫藥行業中搶佔一席之地。展望未來,公司需持續關注市場變化,確保產品成功上市及後續銷售策略的有效執行。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37