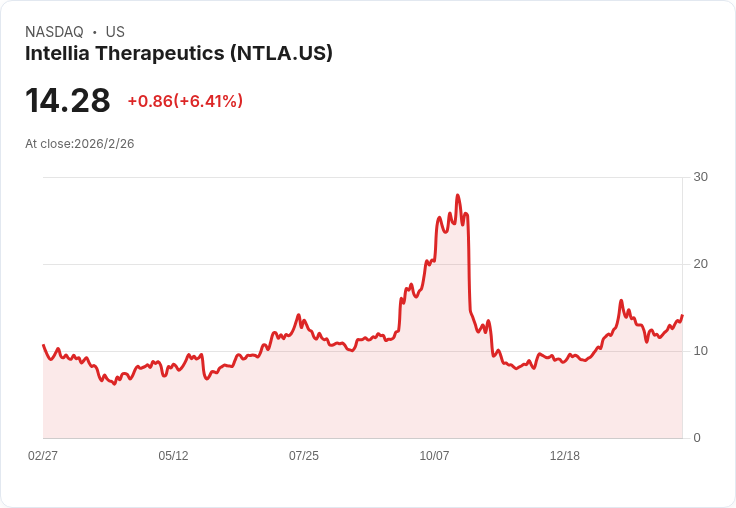
Intellia Therapeutics宣佈將於2026年推出lonvo-z,並在FDA解除MAGNITUDE-2臨床試驗的禁令後,加速商業化準備。
Intellia Therapeutics(NTLA)近日舉行了第四季度財報電話會議,CEO約翰·倫納德強調,經過長達三年的患者跟進研究,尚未見到其主要候選藥物lonvo-z對血清kallikrein和TTR水平的影響減弱。他指出,2025年是公司成就與韌性的一年,並透露遺傳性水腫(HAE)的HAELO III期試驗已完成80名患者招募。根據最新市場調查,99%的受訪者表示若獲批准將考慮使用lonvo-z,而92%的醫療提供者則表示願意開處方。
在談及ATTR澱粉樣變病的MAGNITUDE和MAGNITUDE-2試驗時,倫納德報告稱已有650名患者參加MAGNITUDE,47名參加MAGNITUDE-2。因肝酶升高問題而暫停的MAGNITUDE-2試驗,在2026年1月底獲得FDA解禁,允許重新招募並修訂篩檢和監測方案。首席財務官愛德華·杜拉克表示,公司正在擴大銷售團隊、確定美國治療中心以及最終定價策略,為即將來臨的產品推出做好準備。
展望未來,倫納德預期將在今年中期獲得lonvo-z的頂線資料,並計畫在下半年提交生物製劑上市申請(BLA)。管理層重申,lonvo-z的商業推出仍定於2027年上半年。至於財務狀況,截至2025年12月31日,公司現金及等價物總額為6.051億美元,足以支援未來重要里程碑,包括MAGNITUDE的重新招募和lonvo-z的上市。
儘管分析師對患者安全和監管時間表提出疑問,但整體情緒偏向正面。隨著MAGNITUDE-2禁令的解除,管理層顯示出更大的信心,並專注於推動主要項目的進展,以改變公司的財務和戰略走向。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37