中國核准Exdensur治療成人鼻息肉,基於ANCHOR試驗資料,助GSK強化在華呼吸醫療佈局。
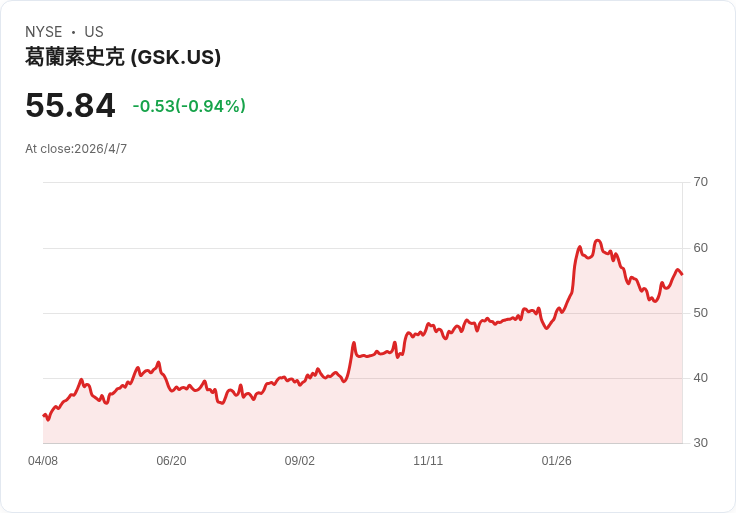
英國藥廠GSK plc(GSK)宣佈,中國已批准其單株抗體藥物Exdensur(通用名depemokimab)作為成人慢性鼻竇炎合併鼻息肉(CRSwNP)在類固醇或手術療效不佳患者的補充治療。訊息一出,GSK在倫敦股價應聲上漲約1.3%。
吸睛開場:此項獲批不僅直接回應對難治性鼻息肉患者的臨床需求,也延續GSK近期在中國呼吸領域的拓展步伐——不久前Exdensur已獲批用於12歲以上青少年與成人的重度氣喘。兩項適應症的獲批,顯示GSK在呼吸照護市場的佈局愈加完整。
背景與依據:根據公司說法,此次批准基於ANCHOR臨床試驗結果,該試驗顯示Exdensur在縮小鼻息肉體積與改善鼻阻塞等症狀上,具「臨床意義且具統計學顯著性」的改善。官方說法強調本次適應症鎖定的是對標準類固醇治療或手術無法獲得滿意緩解的成人患者,補足現有治療空缺。
事實與影響分析:就短期反應而言,市場對於藥物進入中國大市場的利多反映在股價上;中長期來看,此批准可能帶動GSK在耳鼻喉與呼吸科醫療通路的協同銷售機會,尤其是當同一藥物已獲氣喘適應症時,對於合併氣喘與鼻息肉的患者管理具整合優勢。對病患端而言,新增生物藥選項有機會改善對傳統療法不敏感者的症狀與生活品質。
潛在挑戰與反駁替代觀點:有人會指出中國市場對高價生物藥的支付與進院使用存在門檻,且同領域已有其他生物製劑佔有一席之地,競爭激烈。對此觀點可回應:首先,Exdensur獲準的適應症明確針對對類固醇或手術療效不佳者,屬明確未滿足醫療需求的子族群;其次,GSK若能在定價、醫院進入與患者潛在分級給付上取得突破,仍有機會取得實質市場滲透。此外,氣喘與鼻息肉雙重適應症有助於提高臨床採用率與長期治療一致性。
結語與展望(行動號召):GSK在華取得雙重呼吸適應症,短期內可觀察其在中國市場的定價策略、納入醫保與醫院採購進度,以及真實世界療效與安全性資料的釋出。投資人與醫療機構應持續關注後續上市後監測(PMS)資料、醫院處方趨勢與競品回應,評估Exdensur對中國呼吸醫療市場與GSK營收的實際貢獻。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37