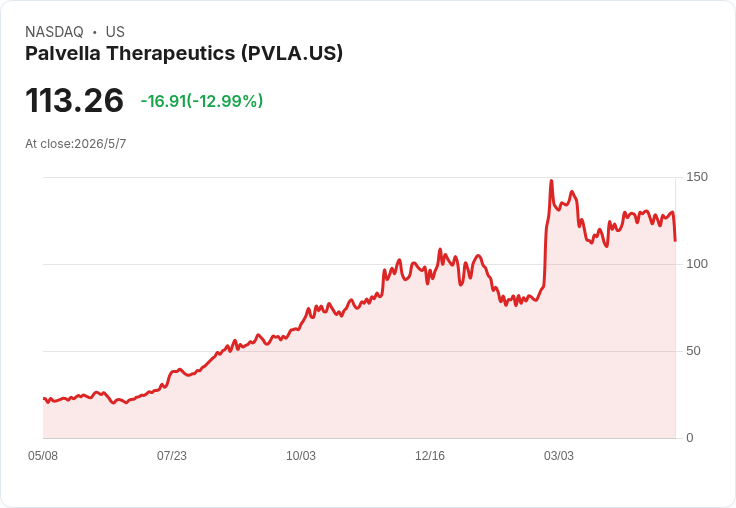
SELVA三期勝利促NDA擬H2 2026遞交,現金261.9M,啟動30–40人拜訪隊伍備戰商業化。
Palvella Therapeutics於Q1財報電話會議上宣佈,旗下區域性雷帕黴素製劑QTORIN在微囊性淋巴管畸形(mLM)之三期SELVA試驗取得「決定性陽性」,公司據此將NDA遞交時程鎖定在2026年下半年,並指出已有美國核准與商業化的路徑與資源佈局。
背景與重點事實 - SELVA三期達成主要與所有預先指定的次要終點,管理層稱此結果支援QTORIN在mLM中的「一線標準治療」定位。公司已獲FDA同意於本季舉行面對面pre‑NDA會議,目標對齊加速提交計畫。 - Palvella估計mLM已診斷患者超過30,000人,並以先前指引的孤兒藥定價區間每位每年10萬至20萬美元,推估QTORIN在美國之高峰銷售潛力超過10億美元。 - 財務面:公司於Q1攜現金及現金等價物261.9百萬美元,完成超額認購的2.3億美元股權融資,管理層表示現金可支援「直到並進入潛在商業化階段」並允許提早投入商業支出。 - 商業與人力部署:擴大啟動規劃包括30–40名外勤業務代表,並已任命Jennifer McDonough、Kent Taylor與CMO Ashley Kline等商業領導。管理層強調「不會資源不足」以支援上市。
管線進度與時間表 - NDA目標:公司重申NDA在2026年下半年遞交目標,並以2027年上半年為潛在美國核准時點。管理層計畫在pre‑NDA會議尋求與FDA對齊、並評估滾動提交等快速通道特色。 - 其他適應症與試驗:皮膚靜脈畸形(cVM)三期預計2026下半年啟動;日光性角化病相關變異(DSAP)二期也在2026下半年;公司規劃在2026年再加入2個疾病線,包括新的QTORIN候選品與QTORIN的第四項適應症。
問答重點與市場認知 - 在投資分析師提問中,公司對關鍵爭點給出回應:其一,關於是否需安慰劑對照試驗,管理層主張各疾病決策不同,mLM具「無自發性緩解」特徵,支援以單臂試驗為主;其二,對於臨床量尺與終點敏感性,Palvella表示會以二期資料鑑別可在三期使用的敏感終點;其三,對於診斷率不足的疑慮,公司啟動BEYOND mLM疾病認知活動以提升診斷與就診率。 - 分析師整體語氣由中性至略偏正面,關注點集中在試驗設計、終點靈敏度、上市假設(病人集中度與滲透率)以及潛在競爭與海外授權可能性。
風險、替代觀點與管理層之回應 - 監管風險:NDA路徑仍有不確定性;公司以「面對面pre‑NDA會議」與探討滾動提交、快速通道功能來緩解。 - 商業執行風險:上市能否覆蓋集中治療中心與高價策略是否成立;公司已籌資擴充套件銷售隊伍並強調不會低估資源需求。 - 臨床與競爭風險:市場上有其他區域性雷帕黴素競爭者在規劃或進行試驗;Palvella回應稱專注於自家產品,並認為FDA核准的標準化藥品可減少臨床使用上的差異性。公司亦以KOL與病人回饋支撐市場接受度的論述(例如調查顯示多數醫師願意採用一線區域性療法)。
深入分析 - 管理層的>10億美元高峰銷售推估基礎是「診斷患者基數>30,000」加上「每位每年10–20萬美元之孤兒藥定價」。但實際達成金額將取決於病人就診率、處方滲透率、保險給付與競爭產品的出現;因此公司所示為上限潛力而非保證。 - Palvella目前具充足現金並完成大型融資,短期內降低了資金瓶頸風險,並能提早投入市場教育與商業化準備;若FDA審評順利,這種「資本+人力」佈局可加速市佔建立。 - 監管關鍵事件包括本季的pre‑NDA會議與2026下半年的提交時程,投資者與市場應密切關注會議紀要與FDA對滾動提交、終點接受度的回應。
總結與展望(行動號召) Palvella將在未來12–18個月面臨數個里程碑:面對面pre‑NDA會議、2026下半年NDA提交、以及潛在2027上半年核准。投資者與業界應關注FDA對單臂資料接受度、公司能否如期完成滾動提交安排、以及ISSVA等學術會議上將披露之個案層級資料。對於關切市場滲透與競爭的讀者,建議密切追蹤公司在診斷率提升、保險給付談判與海外授權動向的進展。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37