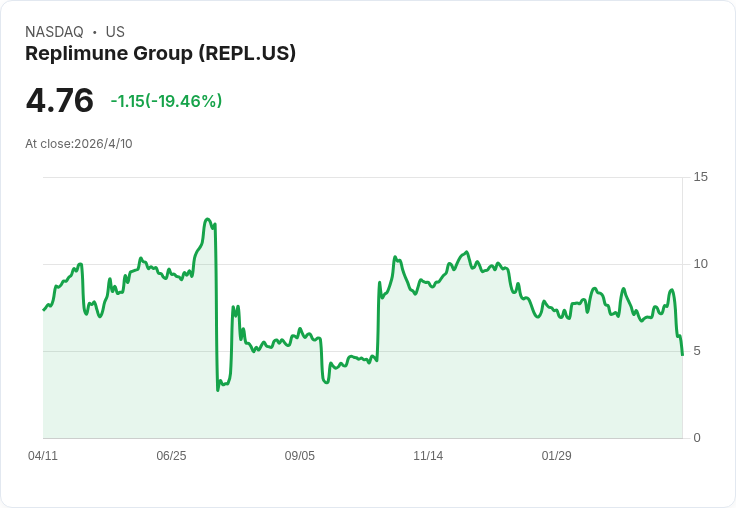
RP1在治療晚期黑色素瘤的BLA遭FDA拒準,Replimune宣佈裁員與縮減美國製造,盤後股價暴跌。
Replimune Group(NASDAQ: REPL)週五證實,美國食品藥物管理局(FDA)對其主力候選藥物RP1發出Complete Response Letter(CRL),公司表示別無選擇,將實施裁員並縮減美國製造業務。訊息公佈後,該股先停牌,盤後股價暴跌約63%,投資人劇烈調整風險評價。
背景與案情核心 RP1為Replimune開發的乏病毒或修飾病毒型免疫療法,該次生物製劑許可申請(BLA)針對RP1聯合百時美施貴寶(Bristol Myers Squibb)之nivolumab(商品名Opdivo),用於晚期黑色素瘤病人在第二線使用。這已是自去年初遭拒後,經公司與FDA進行Type A會議並提出補件說明的一次重要審查關鍵。公司指出本次CRL與FDA先前在Type A會議中對RP1的正面溝通觀點出現矛盾。
公司立場與市場反應 Replimune執行長Sushil Patel表示:「我們對於FDA未展現監管彈性以回應有資料支援的療效與良好安全性深感失望。一項病人迫切需要的治療,並非因藥物失敗而不可及,而是因體制。」公司隨即宣佈將裁減人力並縮減美國製造規模以因應資源重整。投資市場反應強烈,股價於訊息公佈後大幅下挫,顯示投資人對BLA結果與公司財務前景的即時疑慮。
分析:監管與公司角力、風險與替代觀點 從公司角度看,Replimune認為現有臨床資料支援RP1的療效與安全性,FDA應在滿足公共衛生需求下,給予更多彈性或加速通道。相對地,監管機構的立場通常以證據確實性、風險控制與資料完整性為優先;CRL常反映審查團隊對關鍵臨床端點、資料一致性或製造品質等問題仍有疑慮。考量此為第二次主要審查挫折(包含去年7月的先前拒絕),市場與外界亦須評估藥物技術本身、臨床設計是否足以說服監管機構。
事實、資料與案例 - 官方:Replimune已確認FDA發出Complete Response Letter,BLA被拒準。 - 市場:訊息公佈後,REPL盤後股價約暴跌63%,並於當日曾短暫停牌。 - 時序:RP1曾於2025年7月遭初次拒絕;之後雙方於去年進行Type A會議,FDA曾就部分議題有正面溝通,但最終仍發出CRL。
可行因應與未來展望 公司未來路徑可能包含申請與FDA進一步溝通、提出補件或補充臨床資料、申請再會(Type A meeting)或考慮轉向其他適應症、策略性合作或授權以分散風險。但如果短期內無法取得積極進展,資金壓力可能迫使公司進一步縮編、延後或放棄某些研發計畫。對患者端而言,若無藥物獲批,原本期待的治療選項將被延遲或取消。
駁斥替代觀點與結語 針對認為FDA「過於保守」的論點,支持者指出監管審查的嚴謹性旨在避免未證實療法造成廣泛風險;反之,批評者則認為在某些高未滿足醫療需求領域,應有更彈性審查以縮短病人等待時間。無論立場,關鍵仍在於雙方能否就資料缺口達成共識。投資人與病患應關注公司接下來向FDA的溝通進展、是否提出補件或上訴,以及Replimune公佈的裁員規模與資本運用計劃。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37