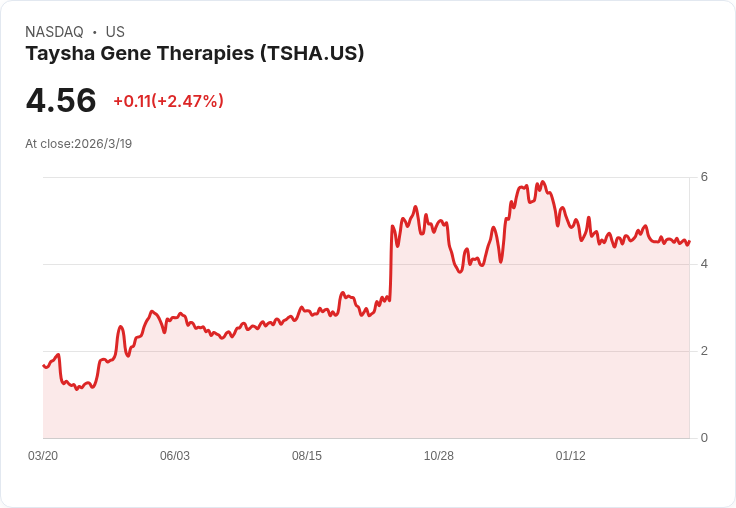
Taysha Gene Therapies CEO Sean Nolan表示,預期在2026年第二季完成關鍵臨床試驗的給藥,並強調其新療法TSHA-102對Rett症候群患者的潛力。
Taysha Gene Therapies正在加速推進其治療Rett症候群的基因療法TSHA-102,CEO Sean Nolan在最新財報會議中指出,2025年是公司執行的重要一年。Nolan提到,REVEAL Phase I/II試驗已經顯示出令人信服的資料,涵蓋兒童、青少年及成人患者,且該療法獲得美國FDA的突破性療法認證。
目前,REVEAL關鍵試驗的多位患者已開始接受治療,初步結果顯示TSHA-102具有良好的耐受性,未觀察到與治療相關的重大不良事件。此療法針對估計有15,000至20,000名患者的根本病因,市場研究也表明,醫生和護理者偏好使用脊髓注射而非直接腦部給藥。
為了增強商業領導團隊,公司任命Brad Martin為市場准入及價值高階副總裁,以支援即將到來的商業化工作。此外,管理層透露,預計在2026年第二季度啟動BLA所需的效能確認批次製造過程,並相信當前資金足以支撐運營至2028年。
然而,隨著研發費用上升至8640萬美元,以及淨虧損達到1.09億美元,分析師們對於公司的商業策略及臨床資料更新提出了一些疑問。儘管如此,整體情緒仍然正面,管理層對於未來的BLA提交持樂觀態度,並期待在下半年分享更多商業戰略細節。Taysha的努力可能在未來為Rett症候群患者帶來新的希望與選擇。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37