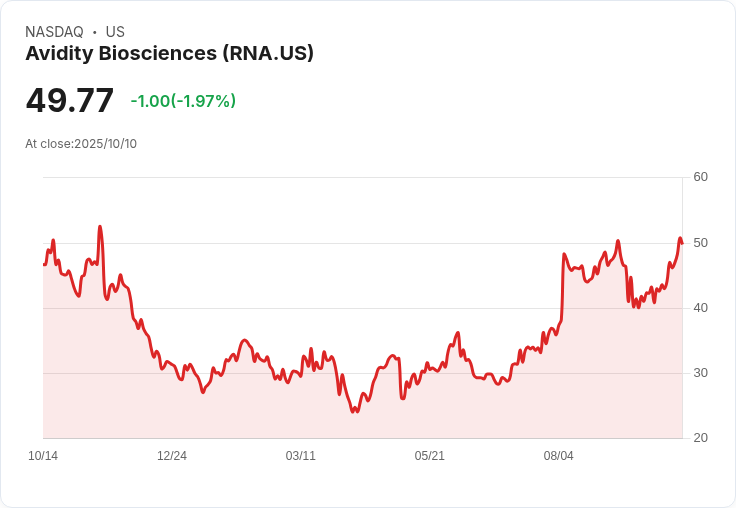
Avidity Biosciences計劃於2026年第一季提交其治療Duchenne肌肉萎縮症的候選藥物del-zota的BLA,並在與FDA的預備會議中獲得了積極反饋。
Avidity Biosciences(NASDAQ:RNA)近日宣佈,在與美國食品藥品監督管理局(FDA)進行的預備生物製劑許可申請(BLA)會議中,其針對Duchenne肌肉萎縮症的候選藥物delpacibart zotadirsen(簡稱del-zota)獲得了正面的評估。原定於2025年底提交的BLA,由於需要提供更多資料以支援化學、製造及控制包裝,因此決定推遲至2026年第一季。
Del-zota已獲得突破性療法認證,專為那些具有適合外顯子44跳過基因突變的Duchenne肌肉萎縮症患者而設計。這一改變不僅反映出Avidity對產品質量的重視,也顯示出他們希望確保在提交時能夠滿足FDA的嚴格要求。
此外,Avidity近期也進行了一項600萬美元的股票發售,以支援其研發計畫。市場對該公司的前景持樂觀態度,多家分析機構維持「強買入」評級,期待del-zota能重新定義Duchenne肌肉萎縮症的治療方式。隨著未來臨床試驗資料的公佈,Avidity有望在這個領域創造新的里程碑。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37