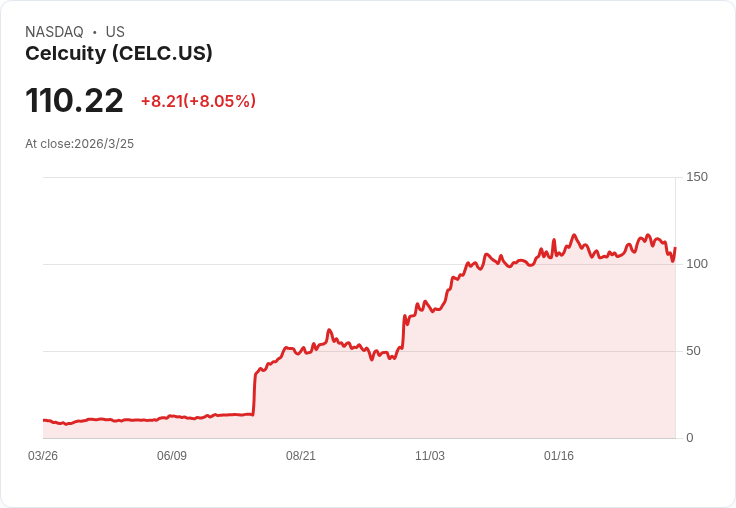
Celcuity 正在為 gedatolisib 的潛在批准和商業化做準備,預計年峰值收入可達 25 億美元,FDA 將於 2026 年 7 月決定。
Celcuity Inc. 執行長布萊恩·沙利文(Brian Sullivan)在最新的財報會議中強調,2025 年將是公司關鍵的一年。該公司正在積極準備「gedatolisib」的潛在批准與商業化,並已獲得美國食品藥品監督管理局(FDA)的新藥申請接受及優先審查,PDUFA 目標日期為 2026 年 7 月 17 日。此外,Sullivan 提到來自 III 期 VIKTORIA-1 臨床試驗的 PIK3CA 野生型群體的前所未有療效資料,預計將於 2026 年第二季公佈 PIK3CA 突變群體結果。
根據臨床資料,「gedatolisib」三重治療的中位無進展生存期達 9.3 個月,相較於僅 2 個月的 fulvestrant,風險比率為 0.24,顯示出其卓越效果。儘管面臨一些安全性問題,但管理層指出該藥物一般耐受性良好,主要的不良事件均為低度。
在商業準備方面,Sullivan 表示,公司已基本完成組織建設,包括銷售團隊和內部系統,以便運作成為商業階段的公司。他估算「gedatolisib」在二線市場的總地址able 市場超過 50 億美元,若兩個群體的正面結果皆如預期,則有望實現高達 25 億美元的年峰值收入。
然而,在金融方面,首席財務官維基·哈恩(Vicky Hahne)報告稱,第四季度淨虧損為 5100 萬美元,每股虧損 0.97 美元,而去年同期為 3670 萬美元、每股虧損 0.85 美元。儘管如此,截至 2025 財年的現金及短期投資仍高達 4.415 億美元,預計足以支援公司運營至 2027 年。
最終,Celcuity 的領導層對於即將到來的 FDA 決策充滿信心,並期待在 2026 年展示更多臨床資料,其商業化路徑也愈加明朗。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37