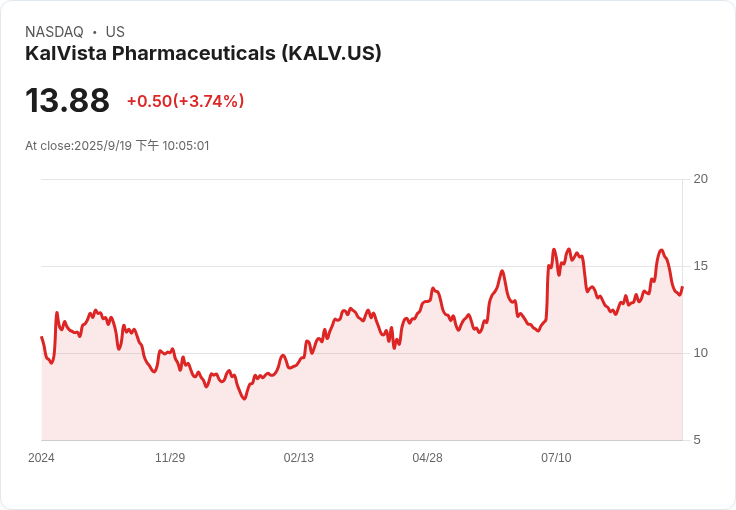
KalVista和Ionis/Sobi獲得歐洲委員會批准,推出針對罕見遺傳疾病的創新治療,為患者帶來希望。
在生物醫藥界的一個重大進展中,KalVista Pharmaceuticals(納斯達克:KALV)和Ionis Pharmaceuticals(納斯達克:IONS)於週五宣佈,歐洲委員會已正式批准他們的兩款針對罕見遺傳疾病的治療藥物。位於麻薩諸塞州劍橋的KalVista表示,其主打產品Ekterly已獲得批准,用於治療遺傳性血管水腫(HAE),這是一種以組織腫脹為特徵的罕見疾病。根據此次批准,Ekterly可作為12歲及以上患者急性發作的口服即時治療藥物。
同時,Ionis及其合作夥伴Sobi也宣佈,他們的抗脂質藥物Tryngolza獲得EU批准,將用於成人飲食配合治療家族性乳糜微粒血癥,這是一種以高甘油三酯為特徵的罕見病症。該決策基於7月專家小組的正面意見,且源自於一項Phase 3平衡研究結果,該研究顯示Tryngolza能在六個月內顯著降低患者的甘油三酯水平。
這些新藥的上市不僅為患者提供了新的治療選擇,也標誌著對罕見疾病認識和治療方法的重要突破。未來,隨著更多臨床資料的累積,這些創新療法有望改善眾多患者的生活品質。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37