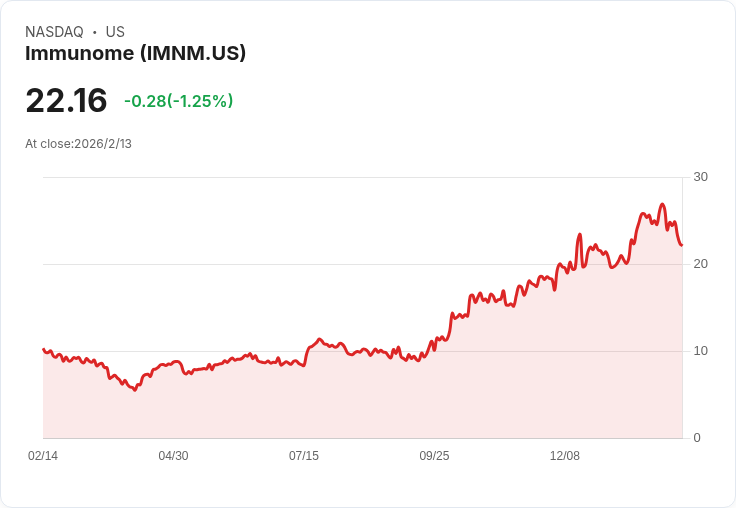
Immunome 在 desmoid 腫瘤的三期試驗中獲得勝利,預計將於數月內向 FDA 提交 NDA,市場潛力可達十億美元。
Immunome, Inc. 的首席執行官 Clay Siegall 強調了公司在腫瘤學領域的進展,特別是在最近的三期臨床試驗中取得的成功。該公司的 gamma secretase 抑制劑 varegacestat 在治療 desmoid 腫瘤上表現出色,超過十個評估指標均顯示積極結果,危險比為 0.16,這使 Immunome 有信心在未來幾個月內提交新藥申請(NDA)。
Siegall 指出,美國每年約有 1,600 例新的 desmoid 腫瘤病例,並且大約 11,000 名患者尋求治療。他認為,若能有效治療這些患者,市場機會可能高達十億美元。此外,Immunome 正在推動其 ADC 專案 IM-1021 的早期階段,已經在多個劑量水平上觀察到客觀反應,並計畫擴充套件至美國和歐洲的試驗地點。
在討論競爭對手時,Siegall 認為 varegacestat 能在多方面脫穎而出,包括更高的客觀反應率、疼痛緩解及一次每日給藥的便利性。他強調醫生與病患對用藥頻率的重視,並指出 Immunome 將持續關注市場需求,以便在批准後吸引更多患者轉換使用他們的新療法。
展望未來,Immunome 計畫在今年提交三項額外的 IND 申請以擴充套件其產品管道,同時啟動放射性配體療法的臨床試驗。這一系列舉措顯示出 Immunome 致力於開發創新療法,並希望在癌症治療領域建立堅實的基礎。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37