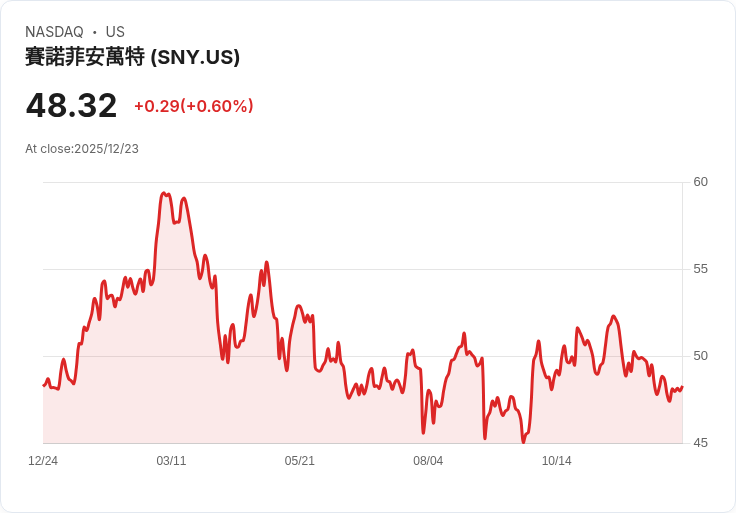
Sanofi的多發性硬化症藥物tolebrutinib在美國遭到FDA拒絕,對未來業務影響深遠。
Sanofi公司於週三宣佈,美國食品藥品管理局(FDA)已針對其多發性硬化症藥物tolebrutinib的上市申請發出完全回應信,正式拒絕該藥物。這一決定是在Sanofi上週表示不會尋求tolebrutinib用於原發性進行型多發性硬化症的批准後作出的,因為該藥物在晚期試驗中失敗。此次被拒的新藥申請主要涉及非復發性次進行型多發性硬化症患者的使用。
根據Sanofi的說法,FDA最近指出,對此布魯頓酪氨酸激酶抑制劑的審查可能會延長至12月18日的目標行動日期之後,並將在2026年第一季度提供進一步指導。Sanofi在宣告中強調,此次拒絕顯示出與之前FDA給予的反饋存在重大差異。他們表示仍然致力於與FDA合作,以尋找推進tolebrutinib的路徑,最終服務於多發性硬化症社群。
此外,Sanofi計劃在1月份公佈第四季財報時,更新有關評估tolebrutinib無形資產價值的減損測試結果,而這一結果將影響公司對2025年的展望。值得注意的是,該公告發布的幾分鐘後,Sanofi還宣佈以約22億美元的全現金交易收購美國疫苗製造商Dynavax Technologies。這些變化都讓投資者對Sanofi的未來充滿了疑慮與期待。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37