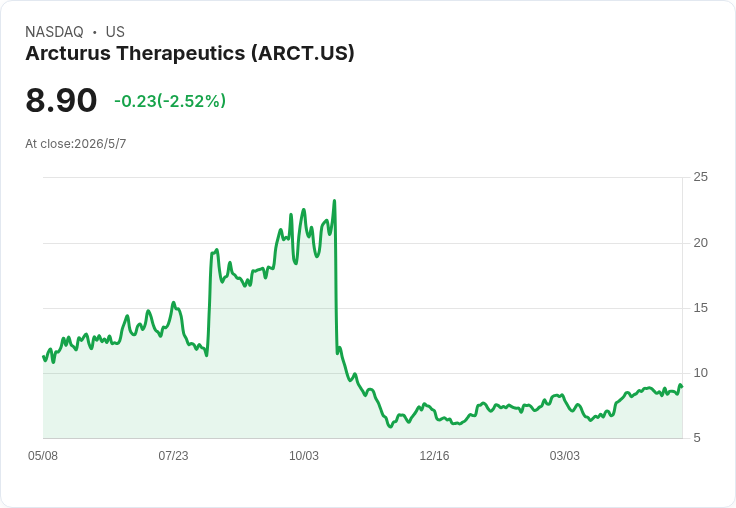
ARCT-032已開始12週開放標籤II期並逾一月用藥,ARCT-810獲Type C會議指引,現金213.4M美元、跑道延伸至2028Q2後。
Arcturus Therapeutics在第1季財報會中宣佈,公司罕見病管線取得實際進展:針對第一型囊性纖維化(CF)的吸入式mRNA候選藥ARCT-032,其12週開放標籤II期在第1季啟動並已超過一個月的重複給藥。執行長Joseph Payne指出,能在臨床上耐受超過一個月的重複吸入給藥,在業界尚屬少見,Arcturus將此歸因於其LUNAR吸入粒子配方與獨特的mRNA純化製程。
背景與試驗設計:首席醫療長Alan Cohen表示,該12週研究以安全性、耐受性為核心,並評估早期臨床益處,包含百分比預測FEV1、肺清除指數(LCI)、兩項經驗證的生活品質量表與高解析電腦斷層影像變化,目標是擴充套件短期給藥以外的資料包。公司同時擴充套件招募至美國以外區域,期望年底前取得足夠入組與中期資料以決定下一步。
財務數據與營運調整:財務長Dennis Mulroy報告,2026年3月31日現金、現金等價物及受限現金為2.134億美元(2025年12月為2.328億美元),並重申公司現金跑道可延伸至2028年第二季以後。第1季營收年減2,730萬美元,主因與CSL的合作收入減少以聚焦罕病計畫;研發費較去年同期減少1,340萬美元,主要來自LUNAR-COVID及BARDA相關製造與臨床成本下降,部分被LUNAR-OTC製造費上升抵消;管理費亦下降180萬美元。
分析與意義:若ARCT-032能在無嚴重耐受性問題下實現持續多週給藥,將是吸入式mRNA朝慢性治療化的重要里程碑,因CF這類疾病可能需要長期反覆給藥。ARCT-810在與FDA的Type C會議後,獲得通往關鍵兒童試驗的較明確法規路徑,並計畫在2026年下半年召開end-of-Phase II會議,對公司短中期估值具正面意義。
替代觀點與駁斥:分析師對ARCT-032的開放標籤設計與無安慰劑對照提出質疑,認為可解讀性與可比性受限。公司回應已設定多項基線與重複性控制,並將取得美國囊性纖維化基金會等大型公開研究作外部參考,以輔助解讀LCI等指標。另有競爭者停止吸入CFTR mRNA試驗的訊息,但管理層強調差異化:例如Arcturus未使用類固醇、獲批可在家中自行給藥,不能簡單類比。
風險提示:主要風險包括入組速度不及預期、關鍵生物標誌物(如尿素生成)仍在發展、以及營收對合作案高度敏感,若合作收入進一步下滑或研發結果不及預期,將壓縮現金流與選擇權。市場情緒短期偏保守,關注可重複性資料與與競品比較。
結論與展望:第1季對Arcturus而言,是從準備進入執行的關鍵轉變——ARCT-032已進入實際給藥期且將於今年內提供更多中期資料,ARCT-810獲得法規明確性並朝兒童關鍵試驗前進。投資者與臨床觀察者應重點關注:1) ARCT-032的LCI與FEV1變化及耐受性資料;2) 年內入組速度與中期解讀;3) ARCT-810的後續法規會議結果;以及4) 公司現金耗用與合作收入變動。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37