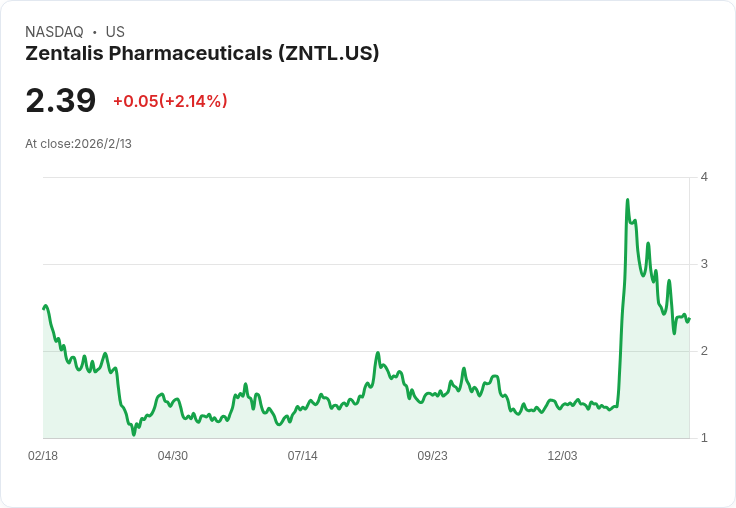
Zentalis制藥計畫在2026年底前報告Azenosertib的臨床結果,並著眼於加速核准其對高cyclin E1表達患者的療效。
Zentalis Pharmaceuticals近期在一次會議中詳細介紹了其WEE1抑制劑Azenosertib針對鉑金抗性卵巢癌(PROC)的加速核准策略。公司總裁Julie Eastland表示,該藥物專為高cyclin E1蛋白表達的患者設計,預計在今年上半年完成DENALI Part 2的登記劑量選擇,並希望在2026年年底之前公佈初步結果。
目前,DENALI Part 2的入組已經完成,共有60名患者參與,根據以往資料,公司設定的目標是30%的整體反應率和5至6個月的反應持續時間。Eastland強調,Azenosertib作為一種口服非化療藥物,有望為患者提供“化療休息”的機會,且相較於抗體-藥物偶聯物(ADC),其安全性資料顯示不良反應可控。
儘管市場競爭激烈,Eastland認為不同治療方法可以共存,特別是在生物標誌物定義的人群中。未來,Zentalis還計畫探索與其他藥物的聯合使用,以滿足更廣泛的醫療需求。隨著關鍵試驗的進展,Zentalis的長期戰略也將逐步明朗。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37