摘要 : 美國FDA接受Telix對腦癌PET造影劑TLX101‑Px的再提交申請,審查期限為2026年9月11日。
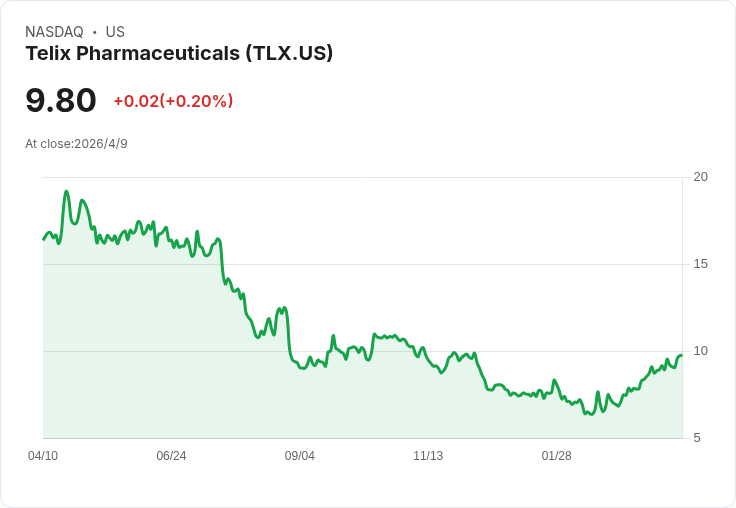
新聞 : 開頭引人注意: 澳洲生技公司Telix Pharmaceuticals(NASDAQ: TLX)宣佈,美國食品藥物管理局(FDA)已接受其對TLX101‑Px(商品名Pixclara)之上市申請。訊息發布後,Telix股價在週五盤前交易中約上漲7%,市場對該影像劑的商業與臨床前景表現出明顯興趣。
背景說明: TLX101‑Px是一種用於正子斷層攝影(PET)的影像候選藥物,目標用於成年人與兒童的復發或進展性膠質瘤(glioma),協助區分腫瘤復發與治療相關變化。該藥品先前一次被FDA駁回,主管機關要求補充關於診斷效能的資料;Telix於上月遞交了補件並獲受理,FDA已將審查目標行動日期(PDUFA-like target action date)訂為2026年9月11日。公司也指出,其2026年的財務展望尚未納入來自TLX101‑Px的任何營收預估。
事實與分析: - 市場反應:股價盤前約+7%反映投資人對審查進展的樂觀;但短期波動不代表最終結果。 - 臨床價值:若能準確區分腫瘤復發與放射治療或其他治療引起的影像變化,TLX101‑Px可改善臨床診斷決策、避免不必要介入治療,對膠質瘤患者具實質臨床意義。 - 經濟與商業面:即便獲準,能否快速轉化為營收仍取決於報銷認可(payor/reimbursement)、醫療機構採用率、產能與定價策略;Telix已明確表示短期財測未將此產品納入收入估計,反映不確定性與保守態度。
替代觀點與駁斥: 有意見認為「FDA受理=核准機率高」,但事實上,受理僅表示申請檔案已完整到可進行實質審查,並不構成批准保證。此前FDA曾以診斷效能資料不足為由拒絕首份NDA,顯示監管要求仍嚴格;審查過程中仍可能要求補充資料、進一步分析或提出風險管理措施。此外,兒童適應症雖提升醫療價值,但也可能使審查更為謹慎。
結論與未來展望(行動號召): TLX101‑Px獲FDA受理是Telix研發程序上的重要里程碑,對患者診斷及公司商業潛力具正面意義,但最終能否獲準、何時獲準以及獲準後的報銷與市佔仍存多重不確定性。建議投資人與醫療界持續關注:FDA在審查期間的進展公告、Telix針對診斷效能的補充資料、以及公司提出的商業化與報銷策略。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37