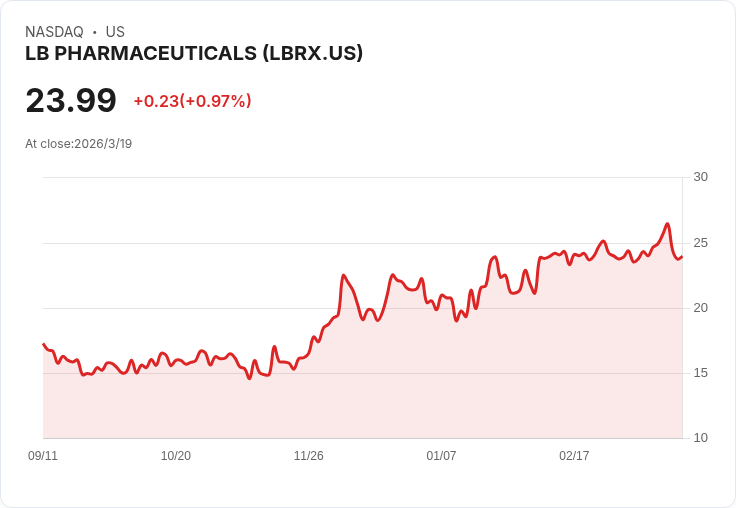
LB製藥宣佈其主要候選藥物LB-102的臨床試驗計劃,並確認公司資金可支援至2029年第二季。
LB製藥(NASDAQ:LBRX)首席執行官海瑟·特納在最近的一次投資者會議中強調,公司正為一系列具臨床意義的價值創造催化劑做好準備。她指出,LB-102針對精神分裂症、雙相抑鬱和輔助性重度抑鬱症等多個精神病學適應症的晚期資料發布將於未來幾年內陸續進行。
根據特納的說法,LB-102的第三階段精神分裂症試驗預計在2027年下半年公佈結果,而第二階段雙相抑鬱症則定於2028年第一季度,輔助性重度抑鬱症的數據則在2029年上半年出爐。該公司已通過PIPE融資確保了到2029年第二季度的資金需求,以支援NDA啟用及安全性研究。
特納詳細介紹了第三階段試驗設計,這是一項三組兩劑量(50毫克和100毫克)的六週研究,旨在降低安慰劑反應風險。她強調,LB-102有望成為美國市場首款無需劑量調整的苯醯胺類抗精神病藥物,其快速見效的特點可能使其在競爭激烈的品牌市場中脫穎而出。
此外,特納還提到,儘管其他產品的推出存在市場懷疑,但LB-102的潛在優勢包括迅速起效及不需要劑量調整。她認為,這些特徵可能成為LB-102成功的關鍵因素,尤其是在面對精神病治療領域的挑戰時。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37