Health Canada 核准 Dr. Reddy’s 司美格魯肽仿製藥,僅限糖尿病適應症,另有8案在審。
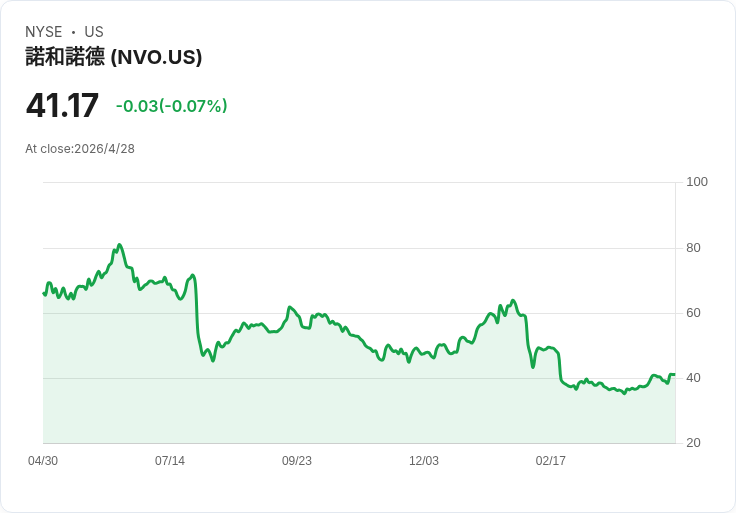
開頭引人: 在全球注視下,加拿大成為首個允許司美格魯肽(semaglutide)仿製藥上市的G7國家——此舉可能成為動搖Novo Nordisk(NVO)以Ozempic/Wegovy稱霸的市場的起點。該仿製藥由Dr. Reddy’s Laboratories獲準,焦點在糖尿病適應症,並未涵蓋諾和針對減重販售的Wegovy適應症。
背景與事實: - 核准機關:Health Canada 已批准 Dr. Reddy’s 的司美格魯肽仿製藥,用於糖尿病治療。 - 範圍限制:此次批准僅限糖尿病指示,並不包含用於減重的Wegovy適應症,意味著減重市場的專屬優勢暫時未被打破。 - 競爭態勢:加拿大主管機關表示另有8份仿製藥申請在審,其中包括Teva Pharmaceutical、Sandoz等業者,顯示未來可能有更多競爭者加入。 - 市場訊號:部分投資研究平臺已對NVO提出風險提示或警示,反映市場正在重新評估其成長與估值風險。
核心分析: 這項批准具有象徵與實務雙重意義。象徵上,作為首個G7案例,加拿大的核准代表監管路徑開始出現裂縫;實務上,因為此次批准僅覆蓋糖尿病適應症,短期內對Wegovy在減重市場的衝擊有限。對Novo Nordisk而言,影響將取決於幾個關鍵變數: - 適應症範圍:若後續仿製藥獲準涵蓋減重適應症,對Wegovy的利潤衝擊會比僅限糖尿病時更劇烈。 - 各國監管節奏:加拿大只是第一步,若歐盟、美國等主要市場相繼放行,全球銷售壓力將快速放大。 - 製造與供應門檻:司美格魯肽為注射型生物藥,生產與品質控管門檻較高,新進者能否以低價快速搶市仍待觀察。 - 價格與市場分配:仿製藥進入通常會造成價格下降與市場分散,但藥廠可透過專利策略、改良配方、品牌醫師關係與給付路徑(reimbursement)維持部分價值。
替代觀點與駁斥: 有觀點認為,單一國家的批准不會立即動搖Novo Nordisk全球營收基礎;確實,短期內NVO仍可倚靠其在多國的市場領先地位與減重適應症的專利保護。然而,反駁此樂觀論據的是:仿製藥申請數量(目前至少8案)顯示市場趨勢已成,多國跟進與跨國法規鬆動只是時間問題;此外,藥價壓力與醫療給付方對成本敏感,長期影響不可小覷。
結論與展望(行動號召): 這一事件是市場競爭走向常態化的訊號,而非一次性偶發事件。投資人與醫療供應鏈參與者應持續關注:其他G7及主要市場的審批進展、各申請案是否擴及減重適應症、專利與訴訟動向,以及仿製藥進入後的價格變化與處方走向。對於持股或評估NVO的投資者,建議檢視公司銷售組合中糖尿病與減重收入的比重、專利到期時間表及管理層應對策略,以調整風險與定價預期。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37