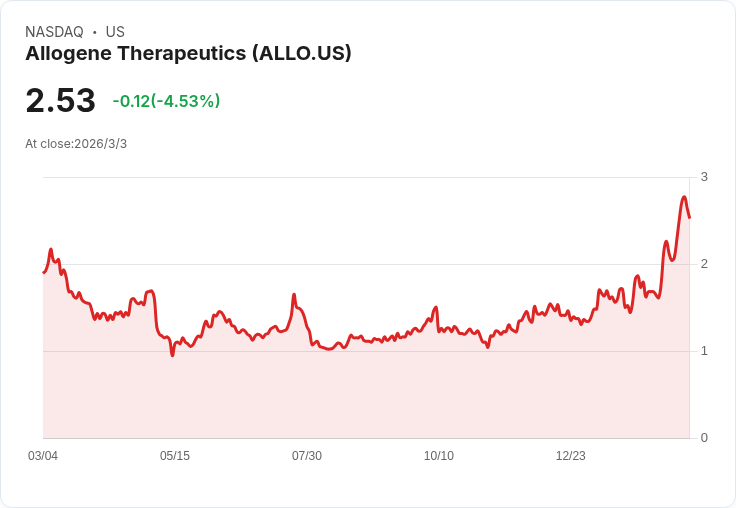
Allogene Therapeutics 在 TD Cowen 大會上透露將於四月公佈 ALPHA3 試驗的中期結果,同時介紹其針對自體免疫疾病的 CAR-T 開發計畫。
Allogene Therapeutics 的總裁兼首席執行官 David Chang 在 TD Cowen 第46屆年度醫療大會上宣佈,公司預計在四月發布 ALPHA3 試驗的中期無效性分析,該試驗專注於前線大型 B 細胞淋巴瘤 (LBCL),並以微小殘留病 (MRD) 清除率為基準。這項隨機研究共招募約220名患者,以事件自由生存(EFS)作為主要終點,目標是達到 cema-cel 與觀察組之間25%-30%的 MRD 清除改善。
Chang 指出,“Allogene XL”全異源 CAR-T 可以以“生物類似”的規模製造,每年產量可達20,000至60,000劑,成本估算在每劑10,000至20,000美元之間。在美國和歐洲,潛在市場約有34,000名 MRD 陽性或治療不足的患者,總地址able market 約5億美元,並預測未來銷售額可能超過20億美元。
此外,Allogene 還介紹了 ALLO-329,自體免疫領域中的雙靶 CD19/CD70 “Dagger” CAR-T,旨在減少或消除淋巴去pletion。初步概念證明及生物標記資料預計將於2026年6月公佈。公司強調安全性與社群癌症中心的交付能力對於此計劃至關重要,並期待四月更新能提供更多資訊。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37