FDA以心臟安全訊號下令全面臨床停試,三期HERO與延伸試驗暫停,公司將解盲並稱現金可支撐營運至2027中。
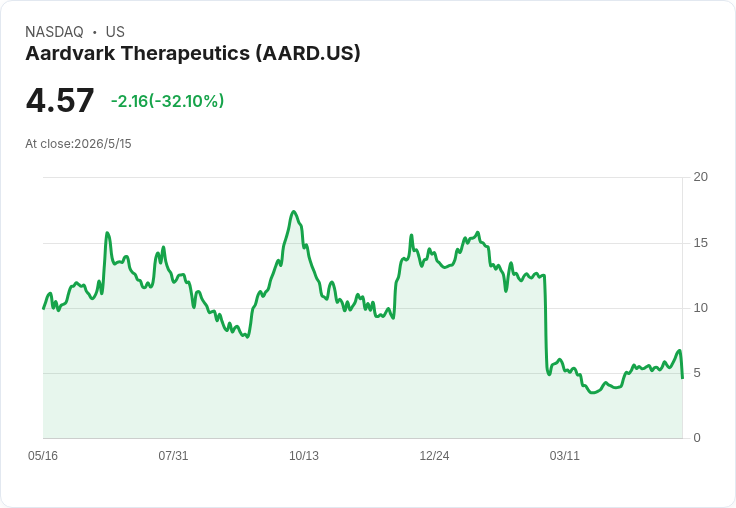
美東時間週五,生技公司Aardvark Therapeutics(代號AARD)股價一度下跌約30%,導火線是美國食品藥物管理局(FDA)對其治療普瑞德–威利症候群(Prader–Willi Syndrome,PWS)飢餓過度症狀藥物候選物ARD-101的臨床試驗提出「全面臨床停試(full clinical hold)」。公司先前已自願暫停試驗,FDA此舉使原本進行中的關鍵三期試驗(HERO)與其開放標籤延伸試驗(OLE)不得不立即停止。
背景與現況: ARD-101為Aardvark針對PWS患者極端食慾(hyperphagia)所開發的創新候選藥物;該適應症為高度未滿足醫療需求,若成功將具重大臨床與商業意義。公司宣告指出,FDA在健康受試者中注意到與心臟相關的安全性訊號,這些訊號可能顯示心臟輸出或效率降低。根據公司資料,截至2月27日,HERO隨機對照試驗已給藥68位患者,OLE則有19位患者參與。
事實與意涵: - 全面臨床停試的法律與實務意義:在FDA解除停試前,該IND下的新試驗不能繼續或新增病人入組;贊助者需向FDA提交補充資料、分析和改善計畫以回應安全疑慮。 - 公司反應:Aardvark表示將對迄今收集的試驗資料進行解盲分析,以評估目前資料的安全性與有效性趨勢,同時強調公司現有現金、現金等價物與短期投資足以支撐營運至2027年中。 - 臨床與監管風險:若心臟安全訊號在解盲後仍屬實,FDA可能要求更多心臟功能資料、延長監測、追加非臨床或臨床安全研究,或修改劑量與入組標準;這將延緩甚至改寫研發時程與潛在上市前景。
深入分析與可能走向: 短期內,Aardvark需完成三件事:1) 內部與外部專家執行詳細的心血管安全性分析(ECG、心肌標誌物、超音波/心臟影像等);2) 向FDA提交完整安全報告與補救計畫;3) 與獨立資料監察委員會或外部心臟專家協調下一步。解盲雖能提供清晰安全/療效訊號,但也可能帶來偏誤風險,影響未來資料解讀與適應症定位。
反駁替代觀點: 部分支持者或投資者可能主張:安全訊號僅出現在健康受試者,可能與基礎疾病群體不同,PWS患者未必會出現同樣問題;且公司有足夠資金續航,短期內並非斷炊。這些觀點雖有其合理性,但FDA下達全面停試通常表示疑慮具體且嚴重;即便資金足夠,監管障礙仍可能導致研發時程大幅延後與成本飆升,且患者與醫療社群會要求透明且嚴格的安全審查。
結論與展望: 目前關鍵在於Aardvark如何迅速且透明地呈交臨床與非臨床安全證據,以及是否能提出可行的風險緩解策略以說服FDA解除停試。對投資人與病友社群而言,未來數週到數月的解盲結果與公司與監管機構的溝通進展將決定ARD-101命運。建議關注公司公告、FDA後續指示,以及獨立專家對心臟安全訊號的評估。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37