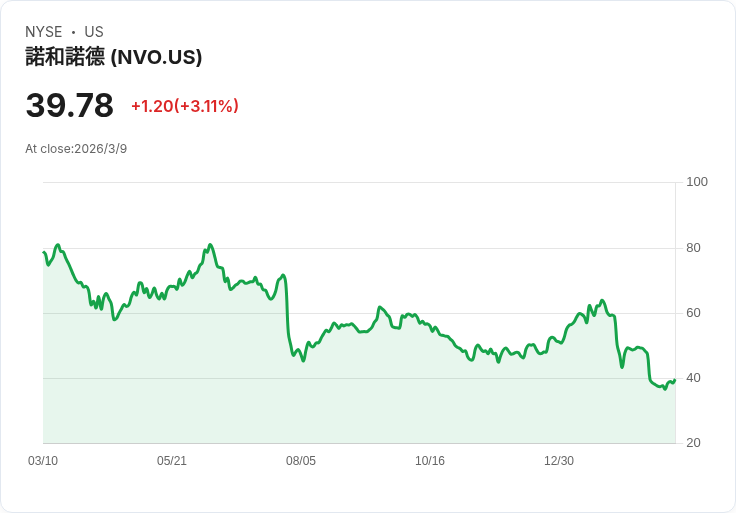
美國FDA對Novo Nordisk發出警告,因其未依規定提交後市不良事件的報告,引發業界關注。
美國食品藥物管理局(FDA)近日向Novo Nordisk發出警告信,指控該公司在後市場不良事件(ADEs)報告方面未能遵循相關法規。此調查於2025年1月至2月進行,結果顯示Novo Nordisk未履行作為持有多種活性成分產品的責任,包括semaglutide和liraglutide等。
根據FDA的信件內容,Novo Nordisk雖然曾多次提供書面回應,但仍被認為未遵從適用的法律要求與規章。FDA指出,Novo需制定書面程式以監測、接收、評估及報告後市場的不良事件。然而,該公司的現有程式並未確保符合所有相關PADE規範。
值得注意的是,semaglutide是減重藥物Wegovy和Ozempic的主要成分,而liraglutide則是Victoza和Saxenda的有效成分。這一警告可能影響Novo Nordisk的市場形象及股價表現,尤其是在競爭激烈的醫療市場中。此外,Novo最近還宣佈將派發DKK 7.95的最終股息,並啟動150億丹麥克朗的股票回購計畫,顯示公司仍在積極尋求增長機會。隨著外部壓力的增加,Novo必須加強合規措施,以避免類似問題再次發生。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37